Butantan espera aprovação da Anvisa para o uso da CoronaVac em crianças
O Instituto Butantan segue com novo pedido à Anvisa para a vacinação de CoronaVac em crianças e adolescentes, após o primeiro ser negado. Nesse novo requerimento, os dados contam com resultados obtidos dos testes feitos em outros países, como China.
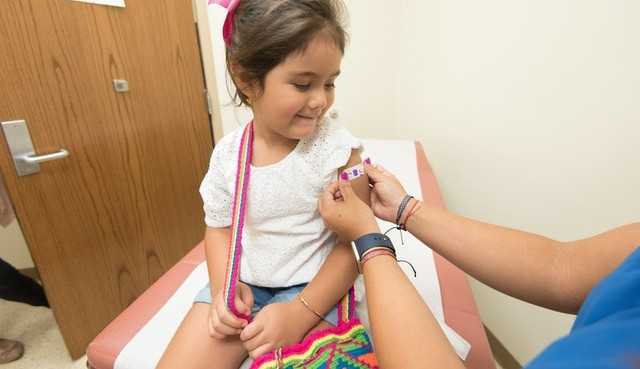
Em novo pedido que planeja ser enviado na próxima semana à Anvisa (Agência Nacional de Vigilância Sanitária), o Instituto Butantan espera autorização para que crianças e adolescentes, entre 3 e 17 anos, sejam vacinados com a CoronaVac. Em agosto, três meses atrás, a agência já havia recusado o primeiro pedido feito pelo laboratório. Na ocasião, os diretores da Anvisa relataram que faltavam informações e solicitaram mais documentos que comprovem a segurança e a eficácia do medicamento nessa faixa etária. Nesse novo requerimento, o Butantan deve ressaltar os resultados da vacinação com a CoronaVac em crianças no Chile e China, países que já autorizaram o uso da Coronavac em crianças a partir de 3 anos.
https://lorena.r7.com/post/Covid-19-Cidade-de-Sao-Paulo-tem-100-da-populacao-adulta-vacinada
https://lorena.r7.com/post/Vacina-da-Pfizer-mostra-100-de-eficacia-em-adolescentes-apos-4-meses
https://lorena.r7.com/post/Cientistas-descobrem-nova-variante-da-Covid-19-com-varias-mutacoes
No dia 09 de novembro, o Butantan já havia divulgado também novos dados sobre a segurança da vacina contra Covid-19 em crianças e adolescentes. De acordo com o Instituto, os resultados preliminares dos testes clínicos de fase 3 que já estão acontecendo na África do Sul, no Chile, nas Filipinas e na Malásia comprovaram que o imunizante é totalmente seguro para crianças e adolescentes entre 3 e 17 anos.
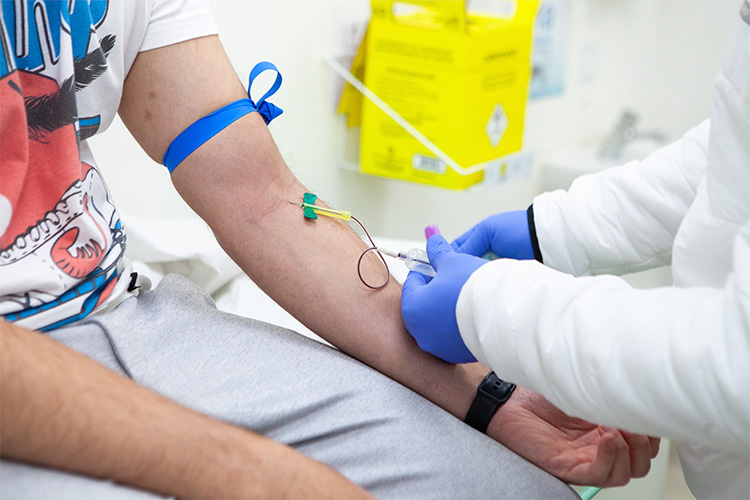
Os testes estão sendo realizados desde outubro e já envolveram 2.140 pessoas com faixa etária de 6 meses a 17 anos. Os estudos ainda continuam para uma melhor avaliação da vacina em bebês de 6 meses a 3 anos. Os dados adquiridos foram administrados pela Sinovac, farmacêutica chinesa responsável pela criação da CoronaVac, e parceira do Butantan no desenvolvimento da vacina no Brasil.
 Criança segurando seringa. (Foto: Reprodução/cottonbro/Pexels)
Criança segurando seringa. (Foto: Reprodução/cottonbro/Pexels)
Segundo as pesquisas do instituto, a vacina é segura e eficaz para essa faixa etária. Os pesquisadores afirmaram que uma resposta imunológica positiva foi observada em 96% dos participantes.
Sobre as reações adversas, segundo as informações divulgadas pelo jornal South China Morning Post, cerca de 18,6% dos voluntários obtiveram. Os efeitos regionais e sistêmicos, incluíam, principalmente, dor no local aplicado e dor de cabeça. Esse resultado foi melhor, comparado com os testes da aplicação das primeiras doses que teve 26,6% de voluntários com efeitos adversos.
Foto destaque: Menina sendo vacinada. Reprodução/CDC/Pexels